This post is also available in .
Wetenschappers werken al decennialang aan de ontwikkeling van therapieën waarbij cellen vervangen worden. Komen we eindelijk vlakbij een doorbraak?
Celvervangingstherapie (Engels: Cell Replacement Therapy ofwel CRT) kan wel eens één van de meest belovende therapieën van de toekomst zijn, die mogelijk hulp biedt bij een scala aan aandoeningen die veroorzaakt worden door slecht functioneren of afsterven van bepaalde lichaamscellen. Een voorbeeld van zo’n ziekte is de ziekte van Parkinson. Wat je vaak ziet bij de ziekte van Parkinson zijn motorische symptomen zoals schudden, trillen en traagheid. Deze worden veroorzaakt door afsterving van een bepaald type cel in de middenhersenen. Normaliter produceren deze cellen dopamine, een stofje dat een rol speelt in signaaloverdracht in het brein. Door deze afsterving is er een tekort aan dopamine in het brein, wat er op zijn beurt weer voor zorgt dat het brein minder goed wordt in het uitvoeren van bewegingen. Echter, in de toekomst kunnen wetenschappers deze cellen wellicht herstellen en patiënten weer op eigen benen helpen met behulp van CRT. Verschillende onderzoeksinstituten zijn momenteel bezig met het opzetten van klinische onderzoeken om te kijken of deze behandelmethode de symptomen van de ziekte van Parkinson kan verlichten. Het is dus de moeite waard om deze therapie en zijn mogelijkheden eens beter te bekijken.
Wat is celvervangingstherapie en hoe werkt het?
Het idee van het vervangen van cellen als therapie (ook wel stamceltherapie genoemd) klinkt vrij eenvoudig. We weten dat celdood in de middenhersenen leidt tot de motorische problemen bij de ziekte van Parkinson, dus waarom proberen we ze niet gewoon te vervangen? Dat zou neerkomen op het plaatsen van gezonde dopamine-producerende cellen in het deel van het brein waar de dode neuronen eerder dopamine produceerden. Onderzoek bij apen met de ziekte van Parkinson heeft laten zien dat getransplanteerde cellen zichzelf volledig kunnen integreren in het brein. De aapjes die de transplantatie hadden ondergaan lieten tot twee jaar hierna minder Parkinson-symptomen zien en meer spontane beweging. Tijdens deze periode overleefden de geïmplanteerde cellen in de apenhersenen en veroorzaakten ze ook geen gevaarlijke effecten in het lichaam.
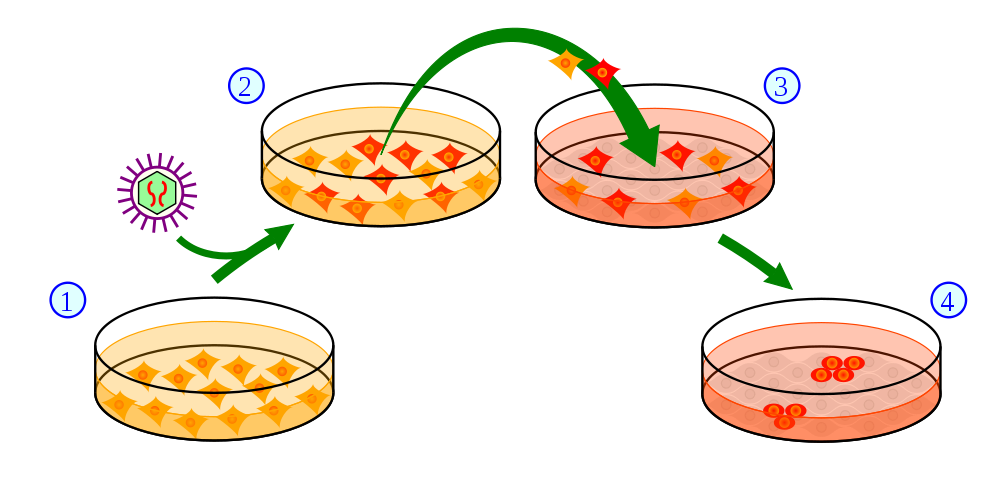
Hoewel er verschillende technieken beschikbaar zijn om nieuwe hersencellen te produceren zullen we hier vooral focussen op een specifieke methode om dopamine-producerende hersencellen te maken die het brein zelf niet meer kan maken. Bij deze methode worden ‘induced pluripotent stem cells’ (ook wel iPS cells genoemd) gebruikt. Een woord-voor-woord analyse van deze term kan ons al een idee geven van wat voor cel dit is. Ten eerste, stamcellen zijn cellen die zich nog kunnen specialiseren in het worden van een bepaald type cel (bijvoorbeeld hersencel, levercel). Het woord pluripotent (pluri = veel, potent = krachtig of effectief) geeft aan dat de stamcel zo goed als elke cel kan worden in het lichaam. Deze kenmerken kunnen door wetenschappers kunstmatig worden veroorzaakt (induced) bij cellen die op een schaaltje groeien. In de meeste gevallen gebruiken wetenschappers volwassen huidcellen van de patiënt zelf en veranderen deze in iPS cellen. Dit wordt gedaan door de geïsoleerde huidcellen aan bepaalde chemicaliën bloot te stellen, die de cellen zo stimuleren dat ze terugkeren naar hun originele niet-gespecialiseerde vorm; een iPS cel. Eenmaal in deze vorm kunnen de onderzoekers deze stamcellen in verschillende soorten cellen transformeren (aan de hand van specifieke informatie wat voor omgeving bepaalde celaanmaak stimuleert). Op deze manier kunnen wetenschappers een patiënt-specifieke transplantaat van dopamine-producerende cellen creëren.
Waarom denken onderzoekers dat dit misschien een veelbelovende therapie is voor de ziekte van Parkinson?
Huidige behandelingen voor de ziekte van Parkinson richten zich op het bestrijden van de symptomen, maar niet op de onderliggende oorzaak van de ziekte. CRT daarentegen richt zich wel op het onderliggende biologische probleem. Het richt zich namelijk op één van de drie cruciale onderdelen die nodig zijn om de ziekte van Parkinson te genezen: een mechanisme dat de ziekte stopt, iets dat verdere schade voorkomt en vervanging van dode cellen d.m.v. CRT. Dat betekent, in plaats van alleen maar de symptomen te onderdrukken, kan CRT wellicht de verdere ontwikkeling van de ziekte tegen kan gaan. Dit zou de dopamine productie weer naar hogere niveaus brengen en beweging verbeteren. Een ander voordeel is dat er weinig risico is op een door het transplantaat veroorzaakte immuunreactie, omdat de cellen van de patiënt zelf komen. Er is daarom geen behoefte aan medicijnen tegen iemands eigen afweersysteem.
Waarom heeft het decennia geduurd om deze techniek te ontwikkelen en is het veilig voor mensen?
Het is belangrijk te benadrukken dat cel-transplantatie bij de ziekte van Parkinson (en andere ziekten) nog in de ontwikkelfase zit. Ook al suggereert het meest recente dieronderzoek dat de procedure veilig is en we over kunnen gaan op humaan onderzoek, kunnen we niet zeker weten dat de therapie geen gevaarlijke bijwerkingen heeft. De grootste zorg rondom CRT, en dan vooral in het brein, is dat de getransplanteerde cellen zich ontwikkelen tot tumoren. Los van dit serieuze risico hebben we ook nog niet het punt bereikt waarop CRT haalbaar is: het maken van iPS cellen is nog steeds een erg duur en lastig. Het op maat maken van deze cellen voor een patiënt kan maanden duren, dus het is niet bepaald een snel proces en daarmee ook niet geschikt voor een grote groep patiënten. Desalniettemin lopen er op het moment drie klinische onderzoeken naar cel-transplantatie bij de ziekte van Parkinson (voor meer informatie klik hier). Het is ook niet zeker hoe goed de CRT-procedure zal gaan werken in Parkinson patiënten, bijvoorbeeld: hoe goed deze cellen zichzelf kunnen integreren in het bestaande netwerk en of alle functies helemaal hersteld kunnen worden. Echter, als je even niet aan al deze nog te overkomen uitdagingen denkt, is er hoop dat deze techniek op een dag het leven van heel veel patiënten zal verbeteren.
Geschreven door Eva, aangepast door Monica, vertaald door Rowena
Afbeelding van Y tambe – Y_tambe’s file, CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=3210604